Luego de que el pasado 11 de agosto el presidente ruso Vladimir V. Putin anunciara con bombo y platillo que científicos rusos habían obtenido “la primera vacuna del mundo contra la COVID-19” –lo que se presumió como un “momento Sputnik”, por el primer satélite artificial de 1957–, tuvo que esperar un mes para convertirse en apenas una simple aspiración a potencial vacuna.
Thank you for reading this post, don't forget to subscribe!Tras las críticas de científicos de todo el mundo, el 4 de septiembre fueron revelados los primeros resultados científicos de la vacuna Sputnik V en la revista The Lancet –una de las más importantes del campo biomédico–, obtenidos entre un grupo muy reducido de personas.
“Entre el 18 de junio y el 3 de agosto de 2020, inscribimos a 76 participantes en los dos estudios (38 en cada uno)”, señala el artículo científico. Es decir, apenas una semana antes del anuncio anticipado de Putin, los investigadores rusos habían terminado de seleccionar a las personas que serían sometidas a los ensayos clínicos Fase 1 y 2.
Sin embargo, antes de tener resultados de las pruebas clínicas las embajadas rusas y la empresa estatal Fondo Ruso de Inversión Directa ya estaban ofreciendo y comercializando su “vacuna” a gobiernos de países del tercer mundo como México, queriendo asegurar un lugar en lo que será un disputado mercado de vacunas contra la COVID-19.
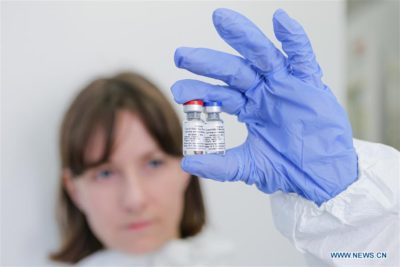
Y han encontrado eco en gobiernos incautos: antes de que se conocieran los resultados de los experimentos científicos y previo a que el propio Ministerio de Salud de la Federación Rusa aprobara el ensayo de Fase 3, el canciller Marcelo Ebrard anunció, el pasado 20 de agosto, que una parte de los ensayos clínicos de la Sputnik V se realizarían en México, con 2 mil participantes.
En el artículo de The Lancet del viernes pasado se indica que el Comité de Ética del Ministerio de Salud de Rusia otorgó el permiso para iniciar el ensayo de Fase 3, entre 40 mil personas, el 26 de agosto.
El artículo titulado “Seguridad e inmunogenicidad de una vacuna COVID-19 primer-impulso heteróloga basada en vectores rAd26 y rAd5 en dos formulaciones: dos estudios abiertos, no aleatorizados de fase 1-2 de Rusia” está firmado por seis científicos rusos encabezados por Denis Y. Lugonov, del Centro Nacional de Investigación en Epidemiología y Microbiología N. F. Gamaleya, de Moscú.
el Comité de Ética del Ministerio de Salud de Rusia otorgó el permiso para iniciar el ensayo de Fase 3, entre 40 mil personas, el 26 de agosto. Seis días antes, el canciller marcelo ebrard anunció que una parte de estos ensayos se realizarían en méxico.
En un solo ensayo abordaron las fases 1 y 2, pero lo hicieron con un grupo muy pequeño: dos conjuntos de 38 personas cada uno, con adultos sanos (hombres y mujeres) de entre 18 y 60 años.
En contraste, la potencial vacuna que desarrolla la Universidad de Oxford se probó en ensayos clínicos de Fase 1 y 2 en 2 mil personas; el Instituto de Biotecnología de Pekín y la empresa CanSino Biological, llevaron a cabo sus ensayos de Fase 2 con 500 participantes; y la empresa Moderna, junto con los Institutos Nacionales de Salud de Estados Unidos, probó la Fase 2 de su vacuna en 600 voluntarios.
Los científicos rusos observaron queque en el 100% de los casos la vacuna producía anticuerpos contra el coronavirus en los 76 participantes, mientras que solo causaba efectos secundarios leves.
Sin embargo, la investigación aún no ha demostrado si las personas que están vacunadas tienen menos probabilidades de infectarse que las que no lo están. Esto se determina en ensayos clínicos de Fase 3 con decenas de miles de voluntarios.
Así actúa la vacuna rusa
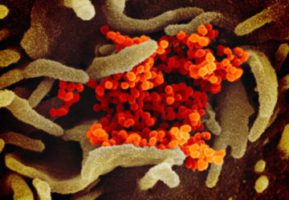
Los investigadores rusos aislaron el gen del SARS-CoV-2 que produce la glicoproteína espiga “S”, que forma las protuberancias que parecen espinas o espigas –que vistas al microscopio le dan la apariencia de corona– y que utiliza el virus para invadir las células humanas. La reprodujeron de manera artificial en el laboratorio.
Luego, tomaron dos adenovirus que ocasionan la gripe común llamados rAd26-S y rAd5-S, y los utilizaron como vehículo para transportar esa proteína al interior de las células humanas. Este enfoque ya lo habían empleado en una vacuna experimental contra el Ébola y es el mismo que usan la Universidad de Oxford y las empresas CanSino y Johnson & Johnson.
La idea es utilizar estos adenovirus como transportadores o vectores del gen que produce la glicoproteína S espiga hasta el interior de las células humanas. Una vez que el adenovirus es inyectado en las células musculares, no hace copias de sí mismo ni causa enfermedades, solo introduce el gen de la proteína S en las células humanas y estas comienzan a reproducir la proteína.
La dosis de la vacuna incluye mil 11 partículas adenovirales que fueron administrados por dos inyecciones intramusculares en el hombro. Estos adenovirus recombinantes invadieron las células de los 76 participantes civiles y militares de los ensayos clínicos.
Todas las vacunas tienen como objetivo exponer al cuerpo humano a ciertos componentes del virus (antígenos) que no causan la enfermedad, pero generan una respuesta del sistema inmunitario del organismo que lo reconoce y produce anticuerpos contra él. De esta manera, cuando el organismo humano se expone al virus real, las células inmunitarias de la persona vacunada están preparadas para combatirlo y prevenir la enfermedad.
La proteina S del coronavirus introducida por los adenovirus es extraña al organismo humano, por ello generó una respuesta inmune en las personas que participaron en los ensayos.
Los voluntarios produjeron anticuerpos que bloquearon la replicación del virus en las células e impidieron el avance de la enfermedad. “Demostramos que los voluntarios que recibieron la vacuna heteróloga rAd26 y rAd5 obtuvieron el mismo nivel de anticuerpos neutralizantes del SARS-CoV-2 que las personas que se han recuperado de la COVID-19”, señalan los científicos.
Las reacciones secundarias más frecuentes fueron dolor en el lugar de la inyección, fiebre, dolor de cabeza, cansancio, dolor muscular y articular, que son típicos de las vacunas basadas en vectores virales recombinantes. No se informaron efectos adversos graves.
Sin embargo, no está claro que la vacuna pueda evitar la infección del virus real; para ello son necesarios los ensayos masivos de Fase 3.
Faltan pruebas masivas
En un artículo publicado en el mismo número de la revista The Lancet realizado por Noar Bar-Zevv y Tom Inglesby, del Centro Internacional de Acceso a Vacunas y del Centro de Seguridad Sanitaria de la Escuela de Salud Pública Johns Hopkins, destacan que el ensayo estableció neutralización completa en los participantes.
Asimismo, indujo amplias respuestas inmunes con una ponderada producción de células T colaboradoras, que son importantes para la seguridad de la vacuna, reduciendo potencialmente el riesgo de enfermedad.
Sin embargo, señalan algunas limitaciones notables del ensayo ruso: en primer lugar, la población que se incluyó en el ensayo es personal militar joven. Es probable que los soldados estén más en forma y más sanos que la población en general. En segundo lugar, en los ensayos no se incluyeron grupos de adultos mayores ni vulnerables, en quienes la vacuna podría ser menos efectiva.
Los investigadores hacen hincapié en la necesidad de realizar pruebas masivas de Fase 3 que contemplen grupos de control y placebo, que aún no se llevan a cabo con la Sputnik V. “Los resultados de seguridad hasta ahora son tranquilizadores, pero los estudios hasta la fecha son demasiado pequeños para abordar eventos adversos graves menos comunes o raros”, indica Noar Bar-Zevv.
Una limitación es que en los ensayos no se incluyeron grupos de adultos mayores ni vulnerables, en quienes la vacuna podría ser menos efectiva.
De hecho, los propios desarrolladores de la vacuna afirman en The Lancet que “se necesitan más investigaciones para evaluar la vacuna en diferentes poblaciones, incluidos grupos de mayor edad, personas con afecciones médicas subyacentes y personas en grupos de riesgo”.
A diferencia de los ensayos clínicos de terapias, en los que la seguridad se equilibra con el beneficio en los pacientes, los ensayos de vacunas deben equilibrar la seguridad con el riesgo de infección, no con el resultado de la enfermedad.
La mayoría de las vacunas se diseñan para atacar la enfermedad y no la infección como tal, pero con la COVID-19 el público podría esperar reducciones sorprendentes en la transmisión de la enfermedad después de la introducción generalizada de la vacuna.
“Tales efectos serían muy bienvenidos si ocurren, pero están lejos de ser seguros”, sostiene Noar Bar-Zevv. “Una vacuna que reduce la enfermedad, pero no previene la infección podría, paradójicamente, empeorar las cosas”.
Todas las candidatas a vacunas deben demostrar seguridad y una eficacia clínica duradera, incluso en grupos de mayor riesgo; para ello se tienen que hacer grandes ensayos aleatorios antes de que se puedan utilizar en la población general y esta es la fase que todavía le falta a la Sputnik V.
De acuerdo con El Panorama de las candidatas a vacunas contra COVID-19 de la Organización Mundial de la Salud del 3 de septiembre, esta vacuna rusa se suma a otras siete que se encuentran en esta etapa de experimentación clínica de Fase 3, entre ellas, cuatro chinas, una inglesa, una estadounidense y otra alemana-estadounidense. Hay otras 14 que están en pruebas con humanos Fase 2; y 12 más, en ensayos clínicos Fase 1.
Independientemente de este artículo científico, todavía no es posible hablar de una vacuna rusa y, por lo tanto, todavía no debería comercializarse, ya que la etapa de experimentación masiva de Fase 3 puede tomar varios meses para producir resultados claros. Ya hay otras siete vacunas más avanzadas por lo que lo más probable es que el “momento Sputnik” nunca ocurrirá.


