Cuba es el único país de América Latina que ha desarrollado su propia vacuna contra la Covid-19, llamada Soberana 2, y se encuentra probando otras cuatro candidatas en ensayos clínicos, entre ellas la Abdala, pero sobre esta última no se han publicado los resultados de sus pruebas Fase 3; a pesar de ello, el gobierno mexicano ya anunció que la comprará y aplicará entre las niñas y niños.
Thank you for reading this post, don't forget to subscribe!Los resultados de seguridad y eficacia de la Fase 3 de experimentación, que se prueban entre miles y decenas de miles personas, son indispensables para que la Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) apruebe una vacuna, pero hasta ahora no cuenta con dichos estudios o, por lo menos, no son públicos como exige la normatividad científica internacional.
Si bien en el Registro Público Cubano de Ensayos Clínicos (RPCEC) existe la anotación de dicha prueba de la Fase 3 de Abdala, no hay ningún documento que avale su seguridad y eficacia. De hecho, en la página web se indica que la última fecha de actualización fue el 4 de abril de 2022 y que la “fecha de próxima actualización” será hasta abril de 2023, pero no hay ningún estudio especializado (Ver: https://rpcec.sld.cu/ensayos/RPCEC00000359-Sp).
Tampoco en el Centro para el Control Estatal de Medicamentos, Equipos y Dispositivos Médicos que es la autoridad reguladora cubana, proporciona resultados sobre el ensayo Fase 3 de Abdala. En la página web del Centro de Ingeniería Genética y Biotecnología (CIGB), donde se desarrolla la vacuna (Consultar: https://www.cigb.edu.cu/news/ensayo-clinico-fase-tres-abdala/) hay información general y de divulgación que explica en qué consiste la vacuna, así como dos artículos científicos uno con los análisis preclínicos y otro de la Fase 1-2, pero no hay ningún artículo científico con los resultados de la Fase 3.
En el registro de RPCEC se indica que se trata de una candidata a vacuna de subunidades de proteína, que se aplica en tres dosis inyectables, y que la Fase 3 se autorizó por las autoridades cubanas el 19 de marzo de 2021, para probarse entre 48 mil 290 personas de entre 19 y 80 años, pero hasta ahora no hay ningún dato del estudio.
el equipo de 30 científicos cubanos informó los resultados del ensayo clínico 1-2 en la revista the lancet. Se probó en 792 personas y obtuvo una eficiencia para prevenir la enfermedad grave y la muerte, del 92%.
Hasta el 9 de septiembre, en el reporte Landscape of candidate vaccines in clinical development (Panorama de las candidatas a vacunas en el desarrollo clínico) de la Organización Mundial de la Salud (OMS), no había ningún informe del resultado de la Fase 3 de Abdala (https://www.who.int/publications/m/item/draft-landscape-of-covid-19-candidate-vaccines).
En este Panorama, la OMS realiza el seguimiento de todas las vacunas y medicamentos contra la COVID-19 que se están desarrollando en el mundo, desde inicios de 2020. Viene el vínculo a la página del RPCEC, pero ningún artículo científico o clínico. En el “Registro de ensayos clínicos de la Unión Europea” tampoco hay ningún registro o artículo (Ver: https://www.clinicaltrialsregister.eu/).
En revistas científicas internacionales no hay ninguna publicación de la Fase 3. El reporte más reciente que existe sobre esta candidata a vacuna fue publicado por los científicos cubanos el pasado 1 de abril de 2022 en la revista The Lancet, pero se trata de los resultados del ensayo clínico Fase 1-2, titulado: Seguridad, tolerabilidad e inmunogenicidad de una vacuna de proteína RBD recombinante del pico del SARSCoV-2: Un ensayo clínico aleatorizado, doble ciego, controlado con placebo, de fase 1-2 (Estudio ABDALA) (Ver: https://doi.org/10.1016/j.eclinm.2022.101383).
En este artículo el equipo de 30 científicos encabezados por Francisco Hernández Bernal, director de Investigación Clínica del CIGB, informa los resultados del ensayo clínico 1-2 probado en 792 personas, entre el 7 de diciembre de 2020 y el 9 de febrero de 2021, que indica que la eficiencia de la vacuna fue del 92%, para prevenir la enfermedad grave y la muerte.
“La vacuna Abdala fue segura, bien tolerada e indujo respuestas inmunitarias humorales contra el SARS-CoV-2. Estos resultados, en el contexto de la pandemia de emergencia por COVID-19, respaldan la dosis de 50 μg, aplicada en un periodo de 0-14-28 días, para realizar más ensayos clínicos para confirmar la eficacia de la vacuna”, informan los científicos en el artículo.
La importancia de la publicación científica
A través de los artículos publicados en las revistas científicas internacionales los expertos del mismo campo de estudio de todo el mundo (y cualquier persona), pueden acceder a toda la información de una investigación como el objetivo, la hipótesis, cómo se llevaron a cabo los experimentos y los resultados, entre otros elementos.
Revistas como Science o PNAS, The New England Journal of Medicine o las del grupo Nature Springer, JAMA, y las de grupos editoriales The Lancet–Elsevier o Cell, entre muchas otras cuentan con cuerpos editoriales compuestos por expertos internacionales que revisan que cada trabajo cumpla con los requisitos de calidad durante todo su desarrollo y examinan que los resultados sean coherentes y replicables. Es la revisión de pares o el arbitraje.
Este es el mecanismo más usual a través del cual se avala o no un trabajo científico. Al publicarse en una revista especializada internacional se puede tener la certeza de que se trata de una investigación fidedigna, confiable, técnicamente robusta y replicable o reproducible.
Por ello, al desarrollarse medicamentos y vacunas los resultados de las diversas fases de experimentación se tienen que publicar en este tipo de revistas. Este requisito es indispensable aún en medio de la urgencia internacional por la pandemia. Todas las vacunas que se encuentran en experimentación y las que han sido aprobadas han publicado los resultados de sus experimentos etapa por etapa, sin excepción.
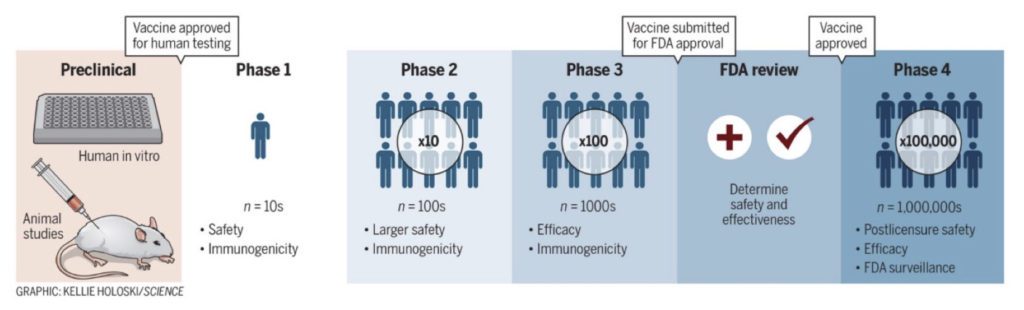
La experimentación de las vacunas se divide en cuatro partes: Preclínica, donde se llevan a cabo experimentos con compuestos, células y animales; la Fase 1 de ensayo clínico, con pruebas en decenas de humanos; la Fase 2 de ensayo clínico, en centenas de voluntarios; y Fase 3, con miles y decenas de miles de personas. En esta última es donde se garantiza la eficiencia y seguridad de la vacuna.
Gracias a las aprobaciones de emergencia ante la pandemia se redujeron los tiempos de prueba de las vacunas, y se pudieron obtener varias de ellas en menos de un año, cuando en tiempos normales tardan entre 5 y 10 años. Pero el requisito de la publicación se mantuvo porque es la única manera de tener la certeza de que una vacuna es segura y efectiva.
Una vez que se hacen públicos los resultados de la Fase 3, las oficinas gubernamentales que aprueban las vacunas en cada país tienen una referencia detallada de los resultados de los experimentos y las pruebas realizadas. Solo así es posible aprobar una vacuna y un medicamento.
Información relacionada:
– Vacuna anti COVID-19 es segura y eficaz en niños de entre 5 y 11 años
– Oculta Conacyt inversión de la vacuna “Patria”
– COVID-19 y vacunación en adolescentes de 12 a 15 años
– Revela Rusia resultados de ensayo 1-2 de su vacuna Sputnik V
– Anuncian vacuna rusa contra COVID-19, pero le faltan pruebas clínicas
– Presentan como “mexicana” vacuna desarrollada y patentada por universidades estadounidenses
– México maquilará la vacuna contra COVID-19 que desarrolla la Universidad de Oxford
Cuba, que padece el embargo económico de Estados Unidos desde hace más de 60 años –incluido el bloqueo de suministros en el campo de salud–, ha tenido que desarrollar su propia biotecnología para producir medicamentos, equipo médico y sus vacunas.
La Soberana 2
A diferencia de la candidata a vacuna Abdala, sobre la vacuna Soberana 2 llamada FINLAY-FR-1A hay información científica disponible de todas las etapas de investigación. Se aplica en tres dosis inyectables y resultó ser segura y eficaz en un 92%. El ensayo de Fase 3 se llevó a cabo con 44 mil 31 participantes, y la eficacia de la vacuna para prevenir COVID-19 grave fue de 100%.
“Nuestros resultados indican que las vacunas SOBERANA, fáciles de fabricar, son eficaces en un contexto de dominancia de COV Beta y Delta y que constituyen una opción atractiva y factible para países de ingresos bajos y medianos, donde además de las limitaciones financieras, la facilidad de almacenamiento y la distribución es motivo de preocupación”, indican los científicos en el estudio publicado en The Lancet, el 27 de julio de 2022 (Disponible en: https://papers.ssrn.com/sol3/papers.cfm?abstract_id=4174293).
También se encuentran los ensayos de Fase 1 de la Soberana 2 publicado en The Lancet Regional Health Americas, el 1 de diciembre de 2021 (Consultar: https://doi.org/10.1016/j.lana.2021.100079) y los resultados del ensayo Fase 2 de la candidata a vacuna Soberana Plus, publicados en The Lancet Respiratory Medicine el 9 de junio de 2022 (https://doi.org/10.1016/S2213-2600(22)00100-X).
Sobre los ensayos de Fase 4 de Abdala que, en teoría, se han llevado a cabo con niñas, niños y adolescentes, tampoco se encuentran los resultados de los estudios clínicos. En el Registro Público Cubano de Ensayos Clínicos (RPCEC) (Ver: https://rpcec.sld.cu/ensayos/RPCEC00000381-Sp) existen datos de la Evaluación de la seguridad e inmunogenicidad del candidato vacunal “ABDALA” en niños y adolescentes donde se indica un ensayo Fase 1-2 entre 592 personas de entre 2 y 18 años que se inició el 20 de agosto de 2021 y que se llevaría a cabo la actualización de la información el 7 de julio de 2022, pero no hay modificaciones.
También se tiene el registro de un estudio de Fase 2 llamado “Meñique”, dirigido a niñas, niños y adolescentes de entre 3 y 18 años, este ensayo se aplicaría en 700 personas y terminaría en diciembre de 2021, pero tampoco hay resultados publicados. (Ver: https://rpcec.sld.cu/en/ensayos/RPCEC00000390-Sp).

Cómo funciona Abdala
Nunca en la historia de la humanidad se han probado y desarrollado tantas vacunas contra un solo patógeno como ahora contra el SARS-CoV-2, de acuerdo con el Panorama de las candidatas a vacunas en el desarrollo clínico de la OMS, hay 199 vacunas en experimentación preclínica (con células y animales) y 172 en ensayo clínico con humanos en Fases 1, 2, 3 y 4.
La razón no es para menos, ya que hasta el día de hoy ha causado la muerte de más de 6 millones y medio de personas de manera oficial, aunque la OMS estima que el número real de fallecimientos es de alrededor de 18 millones, en todo el planeta (ver: https://www.who.int/data/sets/global-excess-deaths-associated-with-covid-19-modelled-estimates).
Contar con vacunas se convirtió en un asunto de seguridad nacional para enfrentar la crisis sanitaria, por ello, Cuba, que padece el embargo económico de Estados Unidos desde hace más de 60 años –incluido el bloqueo de suministros en el campo de salud–, ha tenido que desarrollar su propia biotecnología para producir medicamentos, equipo médico y sus vacunas.
De ahí que los logros en su sistema de salud sean a la altura y por encima de muchas naciones avanzadas, y es el único país de Latinoamérica que tiene la capacidad de desarrollar sus propias vacunas contra la COVID-19 y ya ha inmunizado a prácticamente toda su población.
El país caribeño ha desarrollado la vacuna Soberana 2 y se encuentra probando en ensayos clínicos a las candidatas a vacunas, Abdala, Soberana 1, Soberana Plus y Mambisa. En cambio, en México solo hemos comprado la licencia de uso de la llamada vacuna “Patria” (NDV-HXP-S) –que tiene más de un año y medio probándose por una farmacéutica privada– y que fue desarrollada en Estados Unidos por científicos de la Universidad de Texas en Austin y de la Escuela Icahn de Medicina en Mount Sinai, Nueva York, aunque el gobierno sostiene que es “mexicana”.
Las cinco se basan en la técnica llamada “subunidades de proteína”, una de las más usadas desde hace décadas para fabricar vacunas y es relativamente económica. Con esta técnica, los cubanos han desarrollado varias vacunas contra diversas enfermedades, como hepatitis.
Utilizan una parte de la proteína espiga o de pico (S) del coronavirus que forma la membrana exterior y esos picos que, vistos al microscopio, le dan la apariencia de llevar corona, que usa el virus para adherirse y fusionarse a las células, invadirlas e iniciar el proceso de infección.
La vacuna utiliza una parte de la proteína “S” como antígeno: un agente extraño que, al ingresar al organismo humano es identificado por el sistema inmunitario que responde como un pequeño ejército de moléculas protectoras que generan anticuerpos para neutralizar la amenaza.
Estas vacunas utilizan esta proteína del pico del coronavirus para generar la respuesta inmune; de esta manera, al exponerse al virus real, el sistema inmunitario de la persona vacunada ya está preparado, reconoce a la proteína espiga y neutraliza al coronavirus.
Las vacunas Soberanas son producidas por el Instituto Finlay, el Centro de Inmunología Molecular y el Centro Nacional de Biopreparados, mientras que la Abdala y Mambisa son desarrolladas por el Centro de Ingeniería Genética y Biotecnología (CIGB).